Nesta segunda página já vou colocar a visão que a Medicina Ortomolecular tem a respeito da arterioesclerose, ou aterosclerose. Extraí este texto do livro citado na bibliografia, sem no entanto colocar as propostas terapêuticas do autor. O objetivo disso é manter os méritos do médico americano, respeitar os direitos autorais e abrir espaço para uma nova visão desta tão temida e grave doença. Em outras páginas vou trazer outras opiniões sobre o tema. Boa leitura!

Doenças do Coração: Uma Moléstia Inflamatória [1]
Ouvem-se diariamente alertas sobre a gravidade do problema de colesterol entre os norte-americanos. Como mencionei no Capítulo 2, as doenças do coração são a causa de morte número um nos Estados Unidos. Como eu outrora, você provavelmente aceita o que tais estatísticas e grande parte da mídia sugerem: o colesterol é a causa das doenças do coração.
Nesse caso, talvez você se impressione, como eu me impressionei, ao descobrir que não é o colesterol o culpado pelas doenças do coração, e sim a inflamação dos vasos sangüíneos. Minhas pesquisas revelaram que mais da metade dos pacientes de ataques cardíacos nos Estados Unidos tem níveis normais de colesterol! E adivinhe o que descobri que reduz significativamente ou elimina por completo as inflamações dos vasos sangüíneos. Exatamente: os suplementos nutricionais.
Essa descoberta é revolucionária para o tratamento e a prevenção de ataques cardíacos. Em vez de se concentrar somente em baixar os níveis de colesterol, você precisa entender os passos necessários para diminuir a causa de inflamação em suas artérias. Essa abordagem poderia ter implicações expressivas na prevenção e reversão das moléstias do coração.
E Quanto ao Colesterol?
Você sabia que o colesterol elevado no sangue nem sempre é considerado um fator de risco de doença arterial coronariana ou AVCs? Quando comecei a praticar a medicina, em 1972, considerávamos normal qualquer nível de colesterol abaixo de 320. Lembro-me claramente de dizer a pacientes com níveis de colesterol de 280 ou 310 que não precisavam se preocupar, pois seus níveis estavam normais.
Não foi senão no final dos anos 70 que começamos a perceber que quanto mais alto o nível do colesterol, mais risco havia de um ataque cardíaco ou um AVC. Isso se baseava, em parte, nos estudos de Framingham, que acompanharam os casos de uma grande população de pacientes que viviam em Framingham, Massachusetts. Os cientistas notaram nesses estudos que, conforme subia o nível do colesterol, mais alta era a freqüência de ataques cardíacos. Segundo essa pesquisa, níveis de colesterol acima de 200 seriam considerados anormais e acima de 240 deixariam o paciente sujeito a um alto risco de ataque cardíaco.
No início dos anos 80, os médicos começaram a descobrir que nem todo colesterol era ruim. Aprendemos que o colesterol HDL (High Density Lipoproteins – Lipoproteínas de Alta Densidade) é, na verdade, benigno e, quanto mais alto seu nível, melhor. É o colesterol LDL (Low Density Lipoproteins – Lipoproteínas de Baixa Densidade) que é maligno. O colesterol LDL se acumula junto às paredes das artérias, formando uma placa e estreitando seu lúmen (espaço interno por onde o sangue circula). Já a partícula de HDL tem ação inversa, promovendo uma reabsorção do colesterol depositado na parede da artéria, à medida que passa por esses pontos de acúmulo.
Depois dessa descoberta, começamos não somente a medir os níveis do colesterol como também a determinar as quantidades de colesterol benigno e maligno. Calculamos a proporção dividindo o colesterol total pelo colesterol HDL. Quanto menor essa proporção, melhor se encontra o paciente no que se refere a doenças cardíacas. Hoje é prática comum checar rotineiramente os níveis de colesterol HDL e LDL. Não preciso dizer que todos conhecemos bem a importância do colesterol e dos efeitos detrimentosos do colesterol LDL.
O que compartilhei com você até aqui é do conhecimento comum. Está pronto para o conhecimento incomum?
O colesterol LDL na verdade não é “maligno”. Deus não cometeu um erro quando o criou. O colesterol natural LDL, o tipo que o corpo produz originalmente: é benigno. Na verdade, ele é essencial para formar boas membranas celulares, outras partes das células e muitos hormônios diferentes de que nosso corpo precisa. Não poderíamos viver sem ele. Na verdade, se não o obtivermos a partir de nossa dieta em quantidades suficientes, nosso corpo o produzirá.
Os problemas só começam quando os radicais livres alteram ou oxidam o colesterol LDL natural. Esse colesterol LDL modificado, sim, é “maligno”. Em uma edição de 1989 do New England Journal of Medicine, o dr. Daniel Steinberg postulou que se os pacientes portarem antioxidantes adequados para aplacar a oxidação, o colesterol LDL não se tornará maligno.
Nos anos transcorridos desde o surgimento da teoria do dr. Steinberg, centenas de estudos foram feitos na tentativa de prová-la ou refutá-la. Pode-se deduzir por que cientistas e pesquisadores receberam a nova teoria do dr. Steinberg com tanto entusiasmo. Afinal de contas, dos cerca de 1,5 milhão de ataques cardíacos que ocorrerão somente em um ano nos Estados Unidos, quase metade atingirá pacientes com menos de 65 anos de idade. Todos tivemos amigos ou entes queridos que pareciam gozar de excelente saúde e que morreram subitamente de um ataque cardíaco. Se a teoria de Steinberg se mostrasse verdadeira, portas seriam abertas para uma vasta gama de novos protocolos preventivos e de tratamento.
Em 1997 o pesquisador Marco Diaz fez uma impressionante resenha de todos os estudos que haviam aparecido em publicações médicas de primeira linha desde que o dr. Steinberg apresentou sua teoria. Diaz concluiu que os pacientes com níveis superiores de antioxidantes em seus corpos eram os que menos sofriam da doença arterial coronariana.
Estudos feitos em animais durante esta época também apoiavam a teoria do dr. Steinberg. Os antioxidantes e seus nutrientes de apoio se tornaram a nova esperança na guerra contra nossa matadora número um: as doenças do coração.
A Natureza da Resposta Inflamatória
O colesterol LDL não é o único instigador por trás da inflamação dos vasos sangüíneos. Outras causas principais incluem algo chamado de homocisteína (sobre a qual falarei no Capítulo 6) e os radicais livres que o fumo, a hipertensão, os alimentos gordurosos e o diabetes causam.
A inflamação que ocorre em nossas artérias é muito similar às reações inflamatórias vistas em outras partes do corpo. Tentarei explicar esse processo em termos leigos, para que você compreenda melhor o que realmente ocorre no nível celular. Não se detenha tentando entender as minúcias do processo. (Isso é complicado até para a maioria dos médicos, por isso, não se sinta mal se não compreender tudo.) Explicarei agora qual a melhor forma de prevenir-se contra esse ataque às artérias – o que é na verdade muito simples.
Ao observar a seção em corte de uma artéria típica e de proporções médias (Figura 5.1), você só precisa atentar à primeira camada de células, chamada de endotélio.
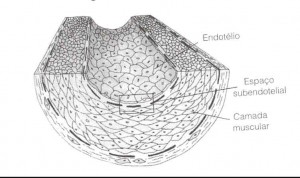
Trata-se do revestimento tecidual fino da artéria. Tudo o que comentarei a seguir envolverá essa fina camada de células e a área logo abaixo dela, chamada de espaço subendotelial (veja a Figura 5.2).
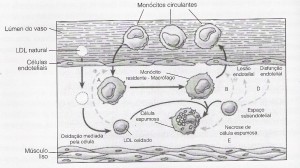
A superfície interna da artéria é composta de uma única camada sensível de células chamada de endotélio, sob a qual encontra-se a camada muscular. Entre o endotélio e a camada muscular está o espaço subendotelial. É onde os danos começam a ocorrer.
O colesterol LDL natural fica preso no espaço subendotelial, onde pode ser facilmente oxidado, se não houver antioxidantes adequados disponíveis. Esse colesterol LDL oxidado é então “engolido” pelos glóbulos brancos macrófagos até que esses fiquem literalmente “estufados” de gordura. Lembre-se de que isso não ocorre se o colesterol LDL não estiver oxidado. Quando o macrófago se estufa com o colesterol oxidado LDL, ele se torna uma “célula espumosa”. A célula espumosa causa danos então ao sensível revestimento da artéria, gerando estresse oxidativo nessa área. Isso provoca lesões e disfunções do endotélio, e o processo de espessamento das artérias tem início. I
A resposta inflamatória é um processo em quatro passos.
Passo 1: O Ataque Inicial ao Endotélio
O endotélio é um revestimento extremamente sensível, vulnerável mesmo à mais ligeira irritação. Quase todos os pesquisadores acreditam hoje que o espessamento das artérias começa quando o estresse oxidativo lesa ou irrita essa camada celular.
O colesterol LDL oxidado, a homocisteína e o excesso de radicais livres provocam o estresse oxidativo que fere o endotélio. Isso ocorre quando o colesterol LDL natural consegue passar para a área abaixo do revestimento da artéria (chamado de espaço subendotelial), onde fica oxidado. Esse colesterol começa então a irritar o revestimento da artéria.
Passo 2: A Resposta Inflamatória
Nosso corpo tem um sistema defensivo projetado para proteger o endotélio da artéria. No caso de ferimento, ele responde enviando certos glóbulos brancos (em maioria monócitos) na tentativa de eliminar o nocivo colesterol LDL oxidado. No local, a equipe defensiva de monócitos se transforma em macrófagos. Essas células começam então a absorver o inimigo na tentativa de minimizar a irritação do endotélio. Se essa resposta inflamatória for bem-sucedida, o problema estará encerrado, e o revestimento da artéria será reparado. Mas não é isso o que costuma ocorrer.
Imagine o macrófago como uma minivan branca. Conforme avança, recolhendo crianças e deixando-as nos lugares adequados, ela está limitada à quantidade de passageiros que consegue carregar simultaneamente, já que tem um número limitado de assentos e de cintos de segurança. Nos dias bons, isso também ocorre com os macrófagos. Quando estamos saudáveis eles giram por aí, recolhendo e liberando colesterol natural LDL. E, assim como uma minivan, os macrófagos só conseguem carregar um número limitado de partículas de colesterol LDL por vez. Isso é conhecido como mecanismo natural de feedback negativo.
Quando o colesterol natural LDL é oxidado, suas partículas deixam de ser crianças inofensivas. Em vez disso, elas representam uma ameaça ao corpo, e os macrófagos os recolhem por um método totalmente diferente. Eles continuam a recolher as partículas delinqüentes de LDL oxidado, mas já não liberam nenhuma. É como uma gangue de jovens extremamente obesos abarrotando-se na minivan pela porta dos fundos, sem que o motorista tenha qualquer controle sobre o número de garotos que entra. Se isso ocorrer, a van ficará imóvel e logo começará a atravancar o trânsito.
Quando encontra o colesterol maligno, o macrófago fica em um apuro similar. Como já não há um mecanismo natural de feedback negativo, ele fica tão abarrotado de colesterol LDL oxidado (gordura) que vira uma célula espumosa. É exatamente o que você está imaginando: uma célula que parece uma bola de gordura. Essa célula espumosa adere então ao revestimento da artéria e acaba gerando o primeiro indício do espessamento das artérias, chamado de estria gordurosa.
A estria gordurosa é uma lesão inflamatória. É o passo inicial no processo chamado aterosclerose. Se o processo simplesmente parasse aqui, o corpo teria ao menos uma chance de eliminar esse defeito. Mas não é esse o caso. Como em qualquer guerra, esse processo provoca algum dano colateral. Em outras palavras, a camada fina e vulnerável de células que reveste nossas artérias é danificada ainda mais pelo próprio processo que deveria curá-la. Isso gera ainda mais inflamação, o que atrai mais macrófagos e converte o colesterol natural LDL em LDL oxidado. Isso provoca uma resposta inflamatória crônica na área em torno do revestimento de nossas artérias.
Passo 3: Resposta Inflamatória Crônica
A inflamação crônica é a causa subjacente de ataques cardíacos, AVCs, doenças vasculares periféricas e aneurismas. Em geral, essas são classificadas como doenças cardiovasculares (doenças que envolvem as artérias de nosso corpo). Quando a inflamação das artérias persiste, a estria gordurosa simples que descrevi começa a mudar. Não somente a inflamação atrai mais glóbulos brancos (sobretudo monócitos), como esses se transformam em macrófagos que continuarão a “engolir” mais LDL oxidado e a se estufarem, formando mais células espumosas. Isso faz surgir uma placa muito mais espessa, e o processo de espessamento das artérias atinge um estádio avançado.
Essa inflamação também gera um estímulo para que as células musculares que com põem a parede da artéria se multipliquem. Essa multiplicação acarreta um maior espessamento da parede arterial, sendo esse processo denominado proliferação. Como resultado, a artéria começa a estreitar-se (veja a Figura 5.3).
Tal processo é um círculo vicioso. Não somente ocorre a geração de uma placa de gordura como também há um espessamento da parede da artéria. Normalmente, o funcionamento da camada endotelial decorre da liberação de um importante produto chamado óxido nítrico. Durante a resposta inflamatória, contudo, a liberação apropriada de óxido nítrico é bloqueada no endotélio, causando seu mau funcionamento. Isso, em contrapartida, faz com que plaquetas adiram à placa e que a artéria ao redor dessa sofra espasmos.
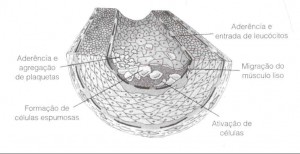
As células espumosas começam a se acumular, atraindo mais monócitos, que acabam se tomando eles próprios células espumosas. O músculo liso passa a proliferar e também a migrar para essa área, sendo que o lúmen da artéria começa a se estreitar. O revestimento da artéria toma-se menos eficaz, o que promove maior estreitamento devido aos espasmos da artéria e à aderência de plaquetas.
Passo 4: A Ruptura da Placa
O evento final em cerca de 50% dos ataques cardíacos é a ruptura de uma dessas placas acarretando a formação de um coágulo ao redor dessa placa rompida. Uma situação como essa provoca um fechamento agudo, abrupto e total dessa artéria, bloqueando o fluxo sangüíneo para aquela parte do corpo. Placas potencialmente perigosas são, com freqüência, pequenas e podem até não causar um estreitamento significativo da artéria – dificultando o diagnóstico de doenças cardíacas antes da ruptura da placa. (Você pode ver, agora, por que as doenças do coração são tão silenciosas e insuspeitas até que a placa se rompa e bloqueie efetivamente a artéria.) O estresse oxidativo também pode causar a avaria dessas placas, o que leva finalmente a sua ruptura.
As artérias podem continuar se estreitando até o ponto em que ficam ocluídas (fechadas). Algum amigo ou parente seu já teve de injetar contraste nas artérias para descobrir se possuía estreitamentos severos das artérias coronárias? Esses pacientes costumam ter como sintomas dores no peito, ou o que os médicos chamam de angina instável. Em situações como essa, tais médicos abrem os vasos mediante uma angioplastia (dilatação por meio de um pequeno balão introduzido dentro do lúmen da artéria), ou criam um desvio dos bloqueios por meio de cirurgia (pontes de safena ou mamária).
Se tivesse de passar um dia acompanhando um cardiologista ou um cirurgião cardiovascular por um hospital, você logo perceberia que ele passa a maior parte do tempo “apagando incêndios”. Ele costuma tratar pacientes que estão no termo do processo inflamatório, concentrando-se totalmente em tentar salvar uma vida de modo heróico. Não resta muito tempo para ensinar aos pacientes as mudanças de estilo de vida necessárias a retardar ou mesmo reverter essa doença devastadora, evitando, assim, a necessidade futura de seus serviços.
[1] Ray, D. Strand, M.D. O Que Seu Médico Não Sabe Sobre Medicina Nutricional Pode Estar Matando Você. Capítulo 5. Ed. M.Books, São Paulo, 2004.
olá, tenho dois filhos uma menina de 13 anos que aos onze estava com a taxa de colesterol 412 e um filho de 16 que também está com o colesterol dito ruim alto. é hereditario pois meu marido também tem colesterol e tomam medicamento para controle:atorvastatina
Oi, Eliana!
Existem 5 tipos de Hipercolesterolemia, sendo que alguns são exclusivamente genéticos.
Sendo assim, cada caso deve ser avaliado individualmente para verificação da necessidade de dieta específica, exercícios físicos e medicação, quando necessária.
A Hiperlipoproteinemia Tipo I, por exemplo, também chamada de Hipertrigliceridemia Exógena, Lipidemia Familial Ácido Graxo-Induzida, ou Hiperquilomicronemia é uma deficiência congênita relativamente rara da atividade de lipoproteína lipase ou de apolipoproteína ativadora de lipase C-II. Nesse caso, há prejuízo na capacidade de remoção ou maior “clareamento” de quilomícrons do sangue. No seu tratamento o objetivo é a redução dos quilomícrons circulantes para evitar episódios de pancreatite aguda. Uma vez que a hipertrigliceridemia é promovida pela ingestão de gorduras, sejam saturadas, insaturadas ou poliinsaturadas, uma dieta criticamente restrita em todas as fontes comuns de gordura é eficaz. As calorias podem ser suplementadas e a palatabilidade aumentada pelo uso de 20 a 40g de Tgs de cadeia média (C 12 ou menos) por dia. Esses ácidos graxos não são transportados via formação de quilomícron, porém não são ligados à albumina e passam diretamente pelo sistema portal hepático.
Já a Hiperlipoproteinemia Tipo II (Hipercolesterolemia Familial; Hiperbetalipoproteinemia; Xantomatose Hipercolesterolêmica Familial) é um distúrbio genético do metabolismo de lipídios, caracterizado por CT sérico em associação com xantelasma, xantomas tuberoso e do tendão, arcus juvenilis , aterosclerose acelerada e óbito precoce devido a infarto do miocárdio. Esse distúrbio ocorre mais freqüentemente num padrão familial de um gene do-minante com penetrância completa, sendo muito mais grave em homozigotos que em heterozigotos. Parece ser causado por ausência ou deficiência de recep-tores celulares para LDL, resultando num atraso para “clearance” LDL, aumento nos níveis LDL plasmático e acúmulo do colesterol LDL sobre as articulações, pontos de pressão e vasos sangüíneos. Quanto ao tratamento, ao abaixar os níveis de colesterol, os xantomas não muito imponentes cessarão de crescer, regredindo ou desaparecendo. Entretanto, a principal razão da terapia é desacelerar o desenvolvimento prematuro de aterosclerose e diminuir a probabilidade de DAC e infarto do miocárdio. Para elevações leves ou mode-radas de LDL colesterol, uma alteração na dieta usualmente é suficiente e representa o primeiro passo no tratamento. As alterações na dieta devem ser tentadas por pelo menos 6 meses antes da determinação de que também é necessária a administração de fármacos. Para hipercolesterolemia grave (p. ex., CT > 240mg/dL, LDL > 160mg/dL) ou doença familial é apropriada a indicação mais precoce da droga.
Sendo assim, cada caso deve ser avaliado em particular, especialmente analisando-se o que se chama na alopatia de “Risco x Benefício”, ok? Abs.
Com tratar então , ou prevenir que se formem as placas e a inflamação?
Aida: A homocisteína é um aminoácido não essencial que tem sido apontado por alguns como fator independente de doença cardiovascular. Esses autores chegam a classificar a hiper-homocisteinemia como um fator de risco tão importante quanto hipercolesterolemia, hipertensão e tabagismo, além de relatarem ser um fator facilmente modificável. Muitos estudos têm sugerido que níveis de homocisteína superiores a 10 mmol/L são associados com ou predizem o desenvolvimento de doença arterial coronariana, com um risco relativo estimado em 1,4 para cada 5 mmol/L acima de 10 mmol/L. Essa associação entre a homocisteína e a aterosclerose poderia ser explicada por diferentes mecanismos, tais como efeitos sobre o endotélio, sobre a síntese das prostaglandinas ou por aumento na agregabilidade plaquetária. Tais efeitos produziriam alteração nos fatores de coagulação, no sentido de favorecer um estado hipercoagulável (pró-trombótico). A homocisteína é um intermediário formado quando da metabolização do aminoácido essencial metionina. O processo começa com a desmetilação de um intermediário secundário sulfurado da metionina, a S-adenosil-metionina, dando origem à homocisteína. A seguir, seguem-se duas rotas: a primeira regulada pela concentração da vit. B6, que visa a excreção da homocisteína pelos rins, diminuindo sua concentração sérica; e a segunda, responsável pelo retorno da homocisteína a metionina, dependente da concentração de vit. B12 e de folato. Dessa forma, as vitaminas do complexo B são cofatores essenciais no metabolismo da homocisteína, pois ambas as rotas são dependentes desses substratos. A ingestão média diária de homocisteína é da ordem de 10 mmol/L em homens adultos, mas dietas ricas em metionina e pobres em vit.B produzem elevação marcada dos níveis séricos desse aminoácido. Da mesma forma, o gênero masculino, idade avançada, função renal prejudicada e determinantes genéticos aumentam a homocisteinemia. Relação inversa existe com aumento do consumo diário de vitaminas do complexo B e folato, pois suplementação dietética com 0,5 mg/dL pode reduzir os níveis de homocisteína em até 25%. Estudos de caso-controle tem demonstrado presença de hiper-homocisteinemia em pacientes com cadiopatia isquêmica, mesmo naqueles pacientes com poucos fatores de risco clássicos para doenças coronarianas. Esses estudos levantaram a hipótese de que o aumento na ingestão de ácido fólico reduziria os níveis da homocisteína. Nenhum estudo, no entanto, conseguiu demonstrar, de forma definitiva, que a redução nos níveis séricos da homocisteína tem correspondência com uma redução da incidência de eventos cardiovasculares agudos. Sabe-se que aumentos nos níveis séricos da homocisteína são freqüentes nos pacientes com cardiopatia isquêmica, mas a pergunta respondida não é essa, mas sim se aqueles pacientes com níveis aumentados de homocisteína têm aumento na incidência de cardiopatia isquêmica e, em caso positivo, se a redução desses níveis diminui os eventos significativos (morte ou infarto) nestes pacientes. Ainda não está estabelecido se a homocisteína é um marcador ou uma causa para a aterosclerose, de forma que uma recente diretriz do Nutrition Committee of the American Heart Association sugere que não devem ser solicitadas dosagens dos níveis séricos da homocisteína, até que resultados de ensaios clínicos randomizados definam se a redução dos mesmos se traduz em diminuição na incidência nos eventos cardiovasculares. De uma forma geral, forte associação entre os níveis aumentados de homocisteína e aumento dos eventos cardiovasculares foi encontrada apenas em estudos de coorte e de caso controle retrospectivos, de forma que os vieses inerentes a esse tipo de estudo são críticos para a análise desta associação. Tais vieses poderão vir a ser evitados apenas com estudos randomizados com a terapia de redução da homocisteína com ácido fólico, os quais ainda não estão disponíveis. Por ora, qualquer terapia com esse objetivo, ou mesmo, a dosagem dos níveis séricos da homocisteína é, no mínimo, precipitada, até porque sua dosagem requer cromatografia líquida de alta pressão e detecção eletroquímica, com grandes dificuldades metodológicas, tornando complicada a sua utilização clínica.
Estou com uma cunhada que tem eplepsia des de 10 anos de idade. Mais ela tem crises frequentes e toma remdios.
Recentemente ela aparento ter tido uma crise um pouco mais demorada e levamos ela ao Hospita. Ela está enternada e primeiro os Médicos diseram ser um AVC agora diseram ser uma inflamacao no coração. Isso é grave a inflamação pode deixar uma pessoa com sintomas de um AVC. Como devemos agir
Cassia:
Infelizmente não posso auxiliar apenas com estes dados. Eu teria que ver os exames, quadro clínico, etc.
Mas, pela sua pergunta, uma miocardite (inflamação do coração) pode ter muitos sintomas parecidos com um AVC.
A melhor coisa a fazer é descobrir a verdadeira causa e dar o tratamento devido, ok?
Abs.
ola! tomara que esta pagina nao esteja desatualizada.mas gostaria de saber mais sobre hipertensao e de um tratamento natural,ja que nao gosto muito de “remedios de farmacia”.agradeço desde ja a atençao dada.
Wilson:
Melhor que um “tratamento natural” para a hipertensão, é ter um estilo de vida mais saudável:
A menos que haja uma necessidade evidente para uso de terapêutica farmacológica imediata, a maioria das pessoas pode testar a redução de sua pressão arterial através de medidas gerais de reeducação de vida:
– A redução do peso deve ser fortemente encorajada em pacientes obesos. Uma queda da pressão arterial pode ocorrer mesmo antes do peso ideal ser atingido.
– A ingesta de gorduras saturadas deve ser reduzida (gordura animal). As taxas de colesterol e triglicerídeos devem ser objeto de orientação nutricional especializada.
– O consumo de álcool deve ser moderado e o fumo abolido.
– Recomenda-se restrição moderada de sal (sódio)
– A atividade física deve ser estimulada de maneira regular (30 a 60 minutos, 3 a 4 x/semana), dinâmicas (caminhadas, natação, ciclismo, corridas leves) e alguns esportes, de acordo com a capacidade física e condições individuais. Exercícios de maior intensidade, principalmente acima de 35 anos, devem ser precedidos de avaliação cardio vascular e iniciados de forma gradual.
Abs.