Faz mal ao coração
Por essa razão o antiinflamatório Vioxx foi retirado do mercado por seu fabricante [1]
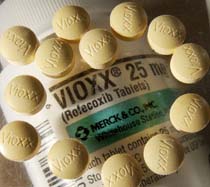
Quando foi lançado, em 1999, o Vioxx foi anunciado como um dos remédios mais eficazes para tratar a dor das vítimas de artrite. Um dos primeiros medicamentos de uma nova classe de antiinflamatórios, os inibidores da enzima COX-2, ele prometia acabar com a dor sem os efeitos colaterais dos remédios antigos, sobretudo as úlceras e os sangramentos gastrointestinais.
O entusiasmo em relação ao remédio foi tão grande que, não demorou muito, o Vioxx passou também a ser receitado para o alívio dos mais variados tipos de dor – de cólicas menstruais a desconforto muscular, de dor de dente a enxaqueca. Consumido por 84 milhões de pessoas em mais de oitenta países, o antiinflamatório transformou-se em um dos carros-chefe do laboratório americano Merck & Co. Só no ano passado, as vendas de Vioxx movimentaram 2,5 bilhões de dólares em todo o mundo.
Na última quinta-feira, essa história de sucesso foi interrompida. Por iniciativa própria, o seu fabricante determinou a retirada do Vioxx do mercado, inclusive o brasileiro. O motivo: o consumo diário de 25 miligramas do remédio, por mais de dezoito meses, dobra os riscos de infartos e derrames. No Brasil, o Vioxx liderava a lista dos antiinflamatórios mais vendidos. Não há, no entanto, razão para pânico. O remédio só aumenta a probabilidade de problemas cardiovasculares se usado continuamente por mais de um ano e meio. E esses casos, segundo a Merck & Co., representam 2% de todas as prescrições de Vioxx.
Até quarenta anos atrás, as experiências com um remédio praticamente se encerravam antes de ele ser lançado. Depois de tragédias como a da Talidomida, as autoridades sanitárias passaram a exigir que os fabricantes fossem mais rigorosos no controle da segurança de seus medicamentos mesmo após sua chegada às farmácias.
A essa vigilância foi acrescentado um outro dado: a fim de garantirem mais alguns anos de exclusividade sobre a patente de remédios lucrativos (caso do Vioxx), os laboratórios começaram a pleitear novas indicações para eles. O alerta para os riscos do Vioxx surgiu justamente a partir de um estudo em que o laboratório testava a eficácia do medicamento contra a recorrência de pólipos em pacientes com histórico de câncer colo-retal.
Em junho de 2000, um estudo da própria Merck & Co. já havia detectado que o Vioxx aumentava o risco de eventos cardiovasculares. Uma das hipóteses mais prováveis é que, ao inibir a ação da enzima COX-2, responsável pela dor e pela inflamação, o remédio estimule a formação de trombos e aumente a pressão arterial. Além do Vioxx, existem outros três medicamentos da família dos inibidores da COX-2. São eles: Celebra, Bextra e Arcoxia. A condenação do Vioxx não é uma sentença contra seus concorrentes, fabricados a partir de moléculas diferentes.
A decisão da Merck & Co. visa não só a preservar a saúde de seus clientes, mas a sua própria. Não havia outro caminho a seguir. Se o laboratório não se pronunciasse, a sua imagem estaria seriamente comprometida e a desconfiança dos consumidores poderia estender-se a todos os seus produtos. Mesmo reconhecendo os riscos do Vioxx, os prejuízos sofridos pela empresa já são grandes. No dia em que o Vioxx foi banido das farmácias, as ações do laboratório despencaram quase 27%.
Concorrentes do Vioxx também trazem riscos, alertam estudos [2]
Drogas antiinflamatórias como o Vioxx, retirado do mercado após descobertas ligações do remédio com problemas cardíacos, podem trazer riscos semelhantes, alertaram dois estudos publicados na última edição do “New England Journal of Medicine”.
A empresa farmacêutica Merck anunciou na semana passada a retirada do Vioxx do mercado mundial, depois que um estudo revelou que seu uso aumenta os riscos de derrames e ataques cardíacos. O remédio é usado no tratamento de artrite e dor.
Publicados duas semanas antes do previsto, os estudos visam informar melhor médicos e pacientes sobre os riscos que representam medicamentos similares ao Vioxx, inclusive o popular Celebrex, do laboratório Pfizer.
A pesquisa, realizada em 1999, quando Vioxx e Celebrex foram aprovados pela FDA (Food and Drug Administration, entidade que regula alimentos e medicamentos nos Estados Unidos), sugere que todos os medicamentos deste tipo têm efeitos semelhantes.
Eles atuam da mesma forma no combate a inflamações, enquanto limitam efeitos colaterais como o mal-estar estomacal, comuns em antiinflamatórios tradicionais. No entanto, neste processo, eles bloqueiam uma substância que ajuda a proteger o coração, afirmou o cardiologista Garret FitzGerald, da Universidade da Pensilvânia (EUA), que conduziu um dos estudos, financiado por duas empresas farmacêuticas.
“Eu acredito que é um efeito desta classe [de medicamentos, que inclui tipos similares, como o Celebrex ou Bextra]”, disse FitzGerald. O Bextra, que chegou ao mercado em 2001, é a nova medicação do laboratório Pfizer para o tratamento da dor.
O cardiologista alertou a FDA para modificar a informação nas embalagens e alertar médicos e pacientes sobre os riscos.
A diretora médica da Pfizer, Gail Cawkwell, disse em um comunicado que “as informações sobre o Celebrex são volumosas e excedem, na proporção de pacientes estudados e na abrangência destes estudos, às informações sobre o Vioxx”.
Uso de antiinflamatório aumenta riscos cardíacos em 40% [3]

Um levantamento de dezenas de estudos demonstrou que o diclofenaco — princípio ativo dos tradicionais remédios Voltaren e Cataflam — pode aumentar em 40% os riscos de ataque cardíaco e morte súbita. O diclofenaco também é vendido como genérico no Brasil.
A informação alarmante foi divulgada nesta terça-feira pela edição on-line da revista “Nature”. Os riscos cardiovasculares da droga são tão graves quanto os apresentados pelo antiinflamatório Vioxx, retirado do mercado há cerca de dois anos.
A revisão sobre as pesquisas anteriores, publicada no “Journal of the American Medical Association”, analisou 23 estudos que envolveram 1,6 milhão de pacientes.
O diclofenaco é uma das substâncias mais receitadas do mundo.
Especialistas entrevistados pela “Nature” informaram que um medicamento equivalente ao diclofenaco que não eleva riscos cardíacos seria o naproxeno.
Em nota, a Novartis, fabricante do Voltaren e Cataflam afirmou que o tipo de estudo realizado “não é aceito pelos órgãos reguladores como evidência clínica para suporte de registro de produto”. A nota afirma ainda que outros estudos científicos não indicam qualquer aumento de risco cardiovascular relacionado ao uso do diclofenaco.
A Novartis afirma ainda que o estudo não levou em consideração dados favoráveis ao remédio e que considera o resultado do estudo questionável. A empresa não pretende retirar os medicamentos de circulação.
Laboratório é acusado de pagar cientistas para assinar estudos sobre o Vioxx [4]
O laboratório norte-americano Merck foi acusado de pagar certos pesquisadores para assinar seus estudos clínicos e artigos sobre o Vioxx, o antiinflamatório retirado do mercado em 2004. A acusação foi feita em estudos divulgados na terça-feira (15).
Vários médicos, entre eles o doutor Joseph Ross, da Faculdade de Medicina Mount Sinai de Nova York, examinaram uma série de artigos publicados sobre o Vioxx (rofecoxib), um antiinflamatório não esteróide relacionado a acidentes cardiovasculares, e concluíram que estudos e testes clínicos eram atribuídos a um conhecido pesquisador que pouco tinha a ver com esses trabalhos.

No artigo publicado no “Journal of the American Medical Association” (Jama) de 16 de abril, os médicos destacam ainda que, nos documentos apresentados pela Merck no julgamento envolvendo o Vioxx, há nomes “contratados” para assinar artigos sobre biomedicina.
“Essa análise da documentação da indústria relacionada ao rofecoxib revela que a Merck recorria sistematicamente à estratégia de utilizar nomes de aluguel para firmar sua literatura médica”, destacam os médicos.
O artigo afirma ainda que a Merck pagava certos pesquisadores para assinar estudos e testes clínicos realizados por outras pessoas. “Esperamos que nosso trabalho promova a discussão sobre como melhorar a integridade da pesquisa médica”, destacou Ross.
“A profissão médica e a indústria farmacêutica deveriam aceitar a idéia de que toda colaboração precisa ocorrer dentro dos mais altos padrões”, concluiu.
Outro lado
A Merck disse em um comunicado que não teve direito de se defender das acusações antes da publicação do estudo. “Nós estamos desapontados por essas declarações falsas e enganosas sobre a Merck feitas por advogados de acusação terem sido publicadas em um periódico médico”, afirmou Peter Kim, presidente da Merck Research Laboratories.

De acordo com a empresa, “uma avaliação imparcial dos documentos da Merck demonstra erros significativos nas conclusões a que chegaram os autores dos estudos do Jama.”
Em 2004, o antiinflamatório Vioxx foi retirado do mercado no mundo inteiro após um estudo ter mostrado o aumento do risco de ataques cardíacos e acidentes vasculares cerebrais.
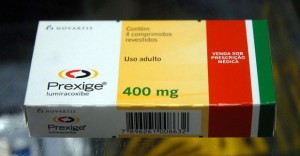
Anvisa proíbe venda dos antiinflamatórios Prexige 400 mg e Arcoxia 120 mg [5]
A Anvisa (Agência Nacional de Vigilância Sanitária) cancelou o registro dos antiinflamatórios Prexige (Lumiracoxibe) 400 mg, do laboratório Novartis, e do medicamento Arcoxia (Etoricoxibe) 120 mg, da Merck Sharp e Dohme. Com isso, fica suspensa a comercialização e o uso dos medicamentos em todo o país.

As novas determinações serão publicadas no “Diário Oficial” da União da próxima segunda-feira (6). Os antiinflamatórios foram suspensos porque especialistas consideram que as reações adversas superam os benefícios. A orientação da Anvisa é para que as pessoas que usam os medicamentos procurem orientação médica para a substituição.
Desde julho, a Anvisa faz testes para verificar a segurança dos antiinflamatórios não esteróides inibidores da Cox-2, enzima que provoca inflamação. Antes, era possível adquirir esse medicamentos com uma receita simples, mas agora a venda só poderá ser realizada com prescrição de receita médica especial e retenção de uma via pela farmácia.
O Prexige é usado no tratamento de artrite, dor aguda e cólica menstrual. Já o Arcoxia é utilizado em casos de reumatismo, gota, artrite, cólica menstrual e no pós-operatório.
Além da suspensão do Arcoxia 120 mg e do Prexige 400 mg, a Anvisa determinou alterações nas bulas do Arcoxia 60 mg e 90 mg, para que o consumidor seja alertado sobre o risco de ter pressão alta e problemas cardiovasculares.
O Celebra (Celecoxibe), da Pfizer, também sofrerá alterações em sua bula. Deverá restringir o tempo de tratamento e o uso durante a gravidez e amamentação. Outro antiinflamatório da Pfizer, o Bextra (Parecoxibe) só poderá ser utilizado em hospitais por causar problemas no estômago e em todo o tubo digestivo.
Outro lado
Em nota, a Novartis afirma que “apesar de acatar imediatamente a decisão”, o Prexige “representava uma opção terapêutica eficaz e segura para o tratamento da dor aguda”.
A empresa também informou que “já vinha voluntariamente reembolsando o valor das unidades devolvidas” do Prexige 400 mg, desde a decisão da Anvisa de suspender temporariamente seu uso e comercialização no final de julho.
“As eventuais unidades que ainda não tenham sido devolvidas serão recolhidas e reembolsadas, de acordo com as determinações da Anvisa”, diz a nota. O telefone do Serviço de Informação ao Cliente da empresa é o 0800-888-30-03.
A Merck Sharp & Dohme lamentou a decisão. “A empresa reitera que a medida não reflete a evidência científica de Arcoxia, baseado em estudos que comprovam o perfil favorável de risco/benefício do medicamento”, afirma em nota.
De acordo com a Merck, os pacientes que tiverem dúvidas sobre a continuidade do tratamento devem consultar o médico ou entrar em contato com a empresa por meio do telefone 0800-012-22-32, de segunda a sexta-feira.
A Pfizer rebateu a decisão da Anvisa. “Pelo fato de os medicamentos Celebra e Bextra injetável sempre terem sido de prescrição médica, a Pfizer considera a medida excesso de rigor e discorda da necessidade de retenção de receita, bem como da restrição de uso de Bextra injetável a hospitais e clínicas”, diz em nota.
“A Pfizer está segura quanto à qualidade, eficácia e tolerabilidade de seus medicamentos e afirma que não há nenhum novo estudo ou dado apontando uma alteração do perfil de segurança de Celebra e Bextra injetável”. O telefone da empresa em caso de dúvidas é o 0800-16-75-75.
Suspensos
Em julho, a Anvisa (Agência Nacional de Vigilância Sanitária) determinou o cancelamento do registro, em todo o país, do antiinflamatório Prexige (do laboratório Novartis) edição 100 mg, e também havia determinado a suspensão, por 90 dias, do produto de 400 mg.
Em agosto do ano passado, a Austrália proibiu o Prexige depois da morte de dois pacientes. Essa medida acabou copiada pelo Canadá e pelo Reino Unido. Em outubro daquele mesmo ano, o FDA (agência reguladora de produtos alimentícios e farmacêuticos), dos Estados Unidos, recusou o remédio.
Também no ano passado, o conselho da FDA (a agência reguladora de medicamentos e comida dos EUA) rejeitou o pedido da farmacêutica Merck para comercializar a pílula Arcoxia, usado como analgésico e antiinflamatório, no mercado americano. O argumento é que o remédio pode aumentar riscos de doenças coronarianas.
Laboratório Pfizer paga multa recorde nos EUA [6]
A Pfizer, maior fabricante de medicamentos do mundo, concordou ontem em pagar uma multa recorde de US$ 2,3 bilhões e encerrar uma ação civil e penal que corria na Justiça dos Estados Unidos.
A empresa é acusada de fazer promoção ilegal de 13 medicamentos. Essa é a maior multa já aplicada pela Justiça americana ao setor de saúde.
Segundo o Departamento de Justiça dos EUA, a Pfizer teria promovido os medicamentos, entre eles o Bextra (anti-inflamatório), o Zyvox (antibiótico), o Geodon (antipsicótico) e o Lyrica (antiepilético), para uso off-label, ou seja, para fins diferentes daqueles para os quais foram aprovados pela FDA (agência reguladora de remédios e alimentos nos EUA).
Os medicamentos são aprovados no Brasil — no caso do Bextra injetável, apenas para uso hospitalar. Segundo a Pfizer, não há ações semelhantes tramitando no país.
No caso do Bextra, que foi retirado do mercado norte-americano em 2005 em razão de riscos cardíacos, a promoção teria envolvido “vários usos e doses que a FDA recusara validar em razão das dúvidas sobre seus riscos”, segundo os autores dos processos nos EUA.

Entre as ações de marketing, havia a informação de que o remédio era indicado para dores agudas e pós-cirúrgicas, enquanto a aprovação da FDA se limitava à dor crônica (tratamento da artrite, por exemplo).
No Brasil, a droga também chegou a ser usada em indicações que não constavam no registro. “Aplicações off-label foram apregoadas e feitas no Brasil”, afirma o reumatologista José Goldemberg, do Hospital Israelita Albert Einstein e professor aposentado da Faculdade de Medicina da Universidade de São Paulo.
No entanto, ele recomenda cautela antes de condenar o uso off-label de um medicamento, argumentando que nem sempre há prejuízos ao paciente.
“O rituximabe, por exemplo, foi desenvolvido para tratar linfoma. Depois, a experiência mostrou que, nas formas graves de lúpus eritematoso sistêmico, seu uso off-label é imbatível. Salvei cinco vidas usando para esse fim. Os remédios off-label têm salvado muita gente quando bem indicados.”
A campanha de promoção do Bextra envolveu ainda viagens de médicos e consultores a resorts luxuosos, pagas pela Pfizer. A ação também foi estendida a médicos brasileiros.
De acordo com Maria José Delgado, gerente de monitoramento e fiscalização de propaganda da Anvisa (Agência Nacional de Vigilância Sanitária), no Brasil é proibida a propaganda de remédios para fins que não constam no registro da droga. “Se o produto é registrado para câncer de mama, não posso dizer que ele cura câncer de próstata”, exemplifica.
Ela argumenta que a propaganda feita diretamente para médicos, nos consultórios ou nos congressos, é mais difícil de ser fiscalizada. “Apesar de ter previsão na resolução de como isso deve ocorrer, é uma relação muito particular e mais difícil de ser monitorada.”
Em janeiro, outra gigante da indústria farmacêutica, a Eli Lilly, havia sido multada em US$ 1,4 bilhão por promoção ilegal do antipsicótico Zyprexa.
Outro lado
O acordo põe fim aos processos civis e penais a respeito. A Pfizer e sua filial envolvida no caso, a Pharmacia & Upjohn Company, pagarão US$ 1,3 bilhão para saldar o processo penal e mais US$ 1 bilhão para concluir o aspecto civil do caso.
“Esses acordos colocam fim a assuntos legais e nos ajudam a focar no que fazemos melhor: descobrir, desenvolver e entregar remédios inovadores para tratar pacientes lidando com algumas das doenças mais debilitantes do mundo”, disse nos EUA Amy W. Schulman, vice-presidente da Pfizer.

“Nos arrependemos de algumas ações do passado, mas estamos orgulhosos das atitudes que tomamos para fortalecer nossos controles internos. Integridade corporativa é uma prioridade absoluta da Pfizer, e nós continuaremos a tomar as ações apropriadas para fortalecer a confiança pública em nossa companhia.”
Ciência, mentiras e Prexige [7]

No momento que escrevo esta coluna, a Anvisa (Agência Nacional de Vigilância Sanitária) acaba de proibir a comercialização no Brasil do antiinflamatório Prexige, da Novartis, seguindo o caminho de agências reguladoras da Europa, Austrália, Canadá e outros países.
Esta proibição se soma à de outros antiinflamatórios da mesma família, a família dos “coxibes”. Ela é composta também, além do lumiracoxibe (nome do produto ativo do Prexige), pelos celecoxibe (Celebra Pfizer), etoricoxibe (Arcoxia Merck Sharp & Dohme), parecoxibe (Bextra IM/IV Pfizer) rofecoxibe (Vioxx Merck Sharp & Dohme) e o valdecoxibe (Bextra Pfizer).
Todos têm em comum que diminuem a inflamação através da inibição de uma substância química produzida pelo nosso corpo, chamada ciclo-oxigenase-2 (ou Cox-2). Dessa família já tinham sido proibidos o rofecoxibe (Vioxx) e o valdecoxibe (Bextra) por terem causado reações adversas graves, inclusive mortes.
Inicialmente acreditava-se que inibindo a Cox-2, apenas aspectos negativos da inflamação, como a dor, seriam eliminados. As pesquisas realizadas pela indústria farmacêutica apontavam que os benefícios dessas drogas seriam bem superiores aos possíveis efeitos colaterais.
Essa idéia foi vendida com muito sucesso através de campanhas de marketing milionárias, que acabaram por convencer quase todos os médicos e dentistas do mundo sobre a conveniência de ministrar esses medicamentos. Mas em poucos anos, muitos usuários começaram a apresentar problemas graves nos rins, fígado e coração, e alguns vieram a falecer.
O primeiro medicamento dessa família a ser proibido foi o Vioxx®. O laboratório que o fabricava, Merck, foi inclusive processado nos Estados Unidos. Das páginas desse processo, surgem informações que dão uma idéia sobre o grau de manipulação de informações à qual estamos sujeitos.
As denúncias partiram de uma das mais prestigiosas revistas de medicina do mundo, o Jama (Journal of the American Medical Association), e quem as faz é nada menos que a Editora Chefe, Catherine D. DeAngelis. É importante esclarecer que o Jama foi várias vezes acusado de proteger a indústria farmacêutica, o que parece afastar objetivos sensacionalistas.

Os artigos foram publicados em julho deste ano. Em um deles, os autores verificaram a prática de “ghostwriting” (autoria fantasma). Trata-se de uma prática na qual um cientista é pago para colocar seu nome em um trabalho científico que foi na realidade escrito por outros que, muitas vezes, nem sequer aprecem como autores.
Em outras palavras, pesquisadores empregados do laboratório realizaram o estudo sob a supervisão da companhia e na hora de publicar, a empresa paga a um cientista famoso para assinar como autor, que presta (vende) assim seu prestígio acadêmico em benefício do produto. De acordo com a Dra. DeAngelis, infelizmente essa parece ser uma prática comum na indústria farmacêutica.
O segundo artigo é ainda mais grave. Acusa a Merck de ter conhecimento que a administração do Vioxx aumentava os riscos de morte em paciente que faziam uso do medicamento. Mesmo assim, o laboratório entregou à FDA (a Anvisa dos Estados Unidos) documentação que, através de manipulação estatística, minimizava esses riscos. As acusações são extremamente graves, e foram feitas -de acordo com a Dra. De Angelis- por que pela primeira vez o Jama tinha provas concretas sobre as mesmas.
Embora não exista bola de cristal, é presumível que em algum tempo todos os inibidores da Cox-2 venham a ser proibidos. Desde a proibição do Vioxx em 2004, importantes periódicos científicos, como o New England Journal of Medicine, já alertavam para a possibilidade de riscos semelhantes ao Vioxx vierem a ocorrer pelo uso de qualquer “coxibe” já que todos agem da mesma forma, bloqueando a Cox-2 que, além do seu envolvimento no processo inflamatório, participa de outros importantes processos biológicos, alguns dos quais, presumivelmente desconhecidos.
Já que nosso sistema de controle e verificação de medicamentos é na melhor das hipóteses precário, seria uma boa medida ficarmos atentos ao que é feito em países que contam com sistemas de farmacovigilância mais aprimorados e eficientes. O lumiracoxibe já tinha sido proibido em 2007 em Austrália, sendo que nem sequer obtivera autorização de comercialização nos Estados Unidos, mas era vendido normalmente no Brasil.
Em relação aos aspectos éticos sobre a participação de médicos e cientistas em esses episódios tão lamentáveis, traduzo as palavras da Dra. DeAngelis: “… se nós não fizermos algo, nossos pacientes continuarão a sofrer as conseqüências. Nós continuaremos a ser manipulados. É hora de tomar de volta nossa profissão. Nós abrimos mão dela, ou permitimos que fossa tirada de nós. Agora temos que recuperá-la. Nada disto teria acontecido se nós não tivéssemos cooperado. Assim de simples.”
[1] Anna Paula Buchalla Veja, Edição 1874, de 6 de outubro de 2004
[http://veja.abril.com.br/061004/p_088.html]
[2] da France Presse, em Washington (EUA) 07/10/2004
[http://www1.folha.uol.com.br/folha/ciencia/ult306u12528.shtml]
[3] 12/09/2006 – da Folha Online
[http://www1.folha.uol.com.br/folha/ciencia/ult306u15175.shtml]
[4] 16/04/2008 – 08h42 da France Presse, em Washington
[http://www1.folha.uol.com.br/folha/ciencia/ult306u392524.shtml]
[5] LÍVIA MARRA, editora de Cotidiano da Folha Online, e TATIANA SANTIAGO, da Folha Online. Com Folha de S.Paulo. 03/10/2008 – 13h54
[http://www1.folha.uol.com.br/folha/cotidiano/ult95u451862.shtml]
[6] CLÁUDIA COLLUCCI – da Folha de S.Paulo – 03/09/2009 – 12h39
[http://www1.folha.uol.com.br/folha/ciencia/ult306u618946.shtml]
[7] Roelf Cruz Rizzolo – Sábado – 02/08/2008 – 03h01 Fonte: Impugning the Integrity of Medical Science: The Adverse Effects of Industry Influence. Catherine D. DeAngelis, CD e Fontanarosa, PB, Jama. 2008;299:1833-1835.
[http://www.folhadaregiao.com.br/noticia?96097&PHPSESSID=2f1ef7915731d8f]

boa materia
muito bom
Yes, correctly.
MUito bom mesmo
É uma pena, porque o Arcoxia tira a dor mesmo, é uma maravilha.
Dr. Paulo, tomei apenas um comprimido do arcoxia e me deu uma dor no lado esquerdo do peito, fui ao cardiologista, fiz até exame de enzimas e graças a deus não deu nada. O médico suspendeu o medicamento e aconselhou tomar novalgina. Porém a dor continua. O sr. poderia me ajudar?
Newton:
Se você tomou apenas um comprimido do Arcoxia, isto não está ligado à dor no peito que você sentiu. Os efeitos colaterais do Arcoxia podem ser: astenia/fadiga, tontura, edema das extremidades inferiores, hipertensão, dispepsia, azia, náusea, cefaléia, níveis elevados de ALT e AST.
O mesmo se refere ao uso da Novalgina.
Se os exames cardiológicos deram normais o seu problema deve ser muscular tipo distensão, entorse ou outro tipo de lesão muscular ou articular.
Procure um Ortopedista ou um bom massoterapeuta, quiropata ou osteopata, ok?
Abs.
Não entendi muito bem.. O Celebra foi ou não proibido no Brasil? Pq a pouco menos de um mês o médico receitou celebra após eu fazer uma pequena procedimento cirúrgico.. Pois após 2hs q tomei o remédio retornei ao hospital passando mto mal.. Com a visão escurecendo.. Suando frio.. Gelada e roxa.. Com a pressão baixa.. Batimentos cardíacos baixo e hipoglicemia.. Acho q por um milagre não morri. O médico suspendeu o celebra e me receitou profenid.
Hiatane, se você com atenção o texto, vai observar o seguinte:
“Além da suspensão do Arcoxia 120 mg e do Prexige 400 mg, a Anvisa determinou alterações nas bulas do Arcoxia 60 mg e 90 mg, para que o consumidor seja alertado sobre o risco de ter pressão alta e problemas cardiovasculares. O Celebra (Celecoxibe), da Pfizer, também sofrerá alterações em sua bula. Deverá restringir o tempo de tratamento e o uso durante a gravidez e amamentação. Outro antiinflamatório da Pfizer, o Bextra (Parecoxibe) só poderá ser utilizado em hospitais por causar problemas no estômago e em todo o tubo digestivo.”
O que você teve, aparentemente, foi uma reação alérgica ao Celebra, que não tem relação com a matéria descrita no texto, ok?
Abs.